“글로벌 3상 임상시험 전략 강화 나서”
젬백스앤카엘은 진행성핵상마비 치료제 GV1001의 개발 및 시장 진입 시기를 앞당기기 위한 개발 전략 구축에 나선다고 16일 밝혔다. PSP는 희귀질환이자 아직 전 세계적으로 개발된 치료제가 없다.
젬백스는 가속 승인 경로를 적극 활용하여 글로벌 3상 임상시험에서 통상적으로 소요되는 임상시험 기간을 단축하거나 조기 시장 진입 등을 위한 방안을 마련하여 미국 내 PSP의 조속한 시장 진입 전략 구축에 집중한다는 계획이다. FDA는 지난 6일 가속 승인 경로에 대한 새로운 지침 초안을 발표했다. 가속 승인은 생명을 위협하는 질환 또는 중대한 질환의 환자에게 의미 있는 치료 대안이 없을 때 새롭고, 안전하고, 효과적인 약물을 신속하게 제공하기 위한 허가심사 제도다.새 지침안 초안에서 주목할 점은 가속 승인의 기준으로 간주하는 평가 변수 중 하나인 임상 변수에 대하여 ‘약물로 의도된 임상적 이득이 예측할 수 있는 중간 임상 평가 지표’로 설명된 부분이다.
중간 임상 평가지표는 비가역적 질병 악화나 사망보다 이른 시점에 측정할 수 있는 치료 효과를 의미하여 이 지표는 해당 약물이 IMM 또는 기타 임상적 혜택에 미칠 효과를 합리적으로 예측할 수 있는 경우 사용한다. 이전 지침에서는 적극적으로 채택하지 않았다. PSP는 치명적이거나 되돌릴 수 없는 수준의 중증 질환으로 가속 승인 대상 질병이다. GV1001의 경우, 최근 국내 PSP 2a상 임상시험 결과에서 질병의 지연 및 근본적 치료 가능성을 보여 글로벌 3상 임상시험을 계획하고 있어 가속 승인 경로를 활용할 수 있을 것으로 기대된다.젬백스 관계자는 “하루빨리 PSP 환자들에게 새로운 치료 옵션을 제공하기 위해 여러 방법을 고민하는 기업의 입장에서 가속 승인 새 지침안은 반가운 소식이다”라며, “임상시험의 효율을 높이고 시장 진입을 앞당길 수 있는 다양한 방안을 통해 세계 최초 PSP 치료제 개발에 성공할 수 있도록 최선을 다하겠다”라고 말했다.
대한민국 최근 뉴스, 대한민국 헤드 라인
Similar News:다른 뉴스 소스에서 수집한 이와 유사한 뉴스 기사를 읽을 수도 있습니다.
 새 의료기기 시장 진입 대폭 단축…안정성·비급여 양산 우려이르면 내년 하반기부터 디지털 치료기기, 인공지능 진단보조기기 등 새로운 의료기기가 임상 안전성·유효성 평가 없이 바로 시장에 진입할 수 있게 된다. 보건복지부와 식품의약품안전처, 국무조정실은 21일 국무총리 주재로 열린 제49회 국정현안관계장관회의에서 이런 내용의 ‘
새 의료기기 시장 진입 대폭 단축…안정성·비급여 양산 우려이르면 내년 하반기부터 디지털 치료기기, 인공지능 진단보조기기 등 새로운 의료기기가 임상 안전성·유효성 평가 없이 바로 시장에 진입할 수 있게 된다. 보건복지부와 식품의약품안전처, 국무조정실은 21일 국무총리 주재로 열린 제49회 국정현안관계장관회의에서 이런 내용의 ‘
더 많은 것을 읽으십시오 »
 더 거세질 무역전쟁 … 부산시 민관협력 경제대응팀 만든다장대환 매경미디어그룹 회장'韓경제 리스크 대응' 제안에'바로 실천' 박형준 시장 화답조선·변압기 산업 수혜 기대
더 거세질 무역전쟁 … 부산시 민관협력 경제대응팀 만든다장대환 매경미디어그룹 회장'韓경제 리스크 대응' 제안에'바로 실천' 박형준 시장 화답조선·변압기 산업 수혜 기대
더 많은 것을 읽으십시오 »
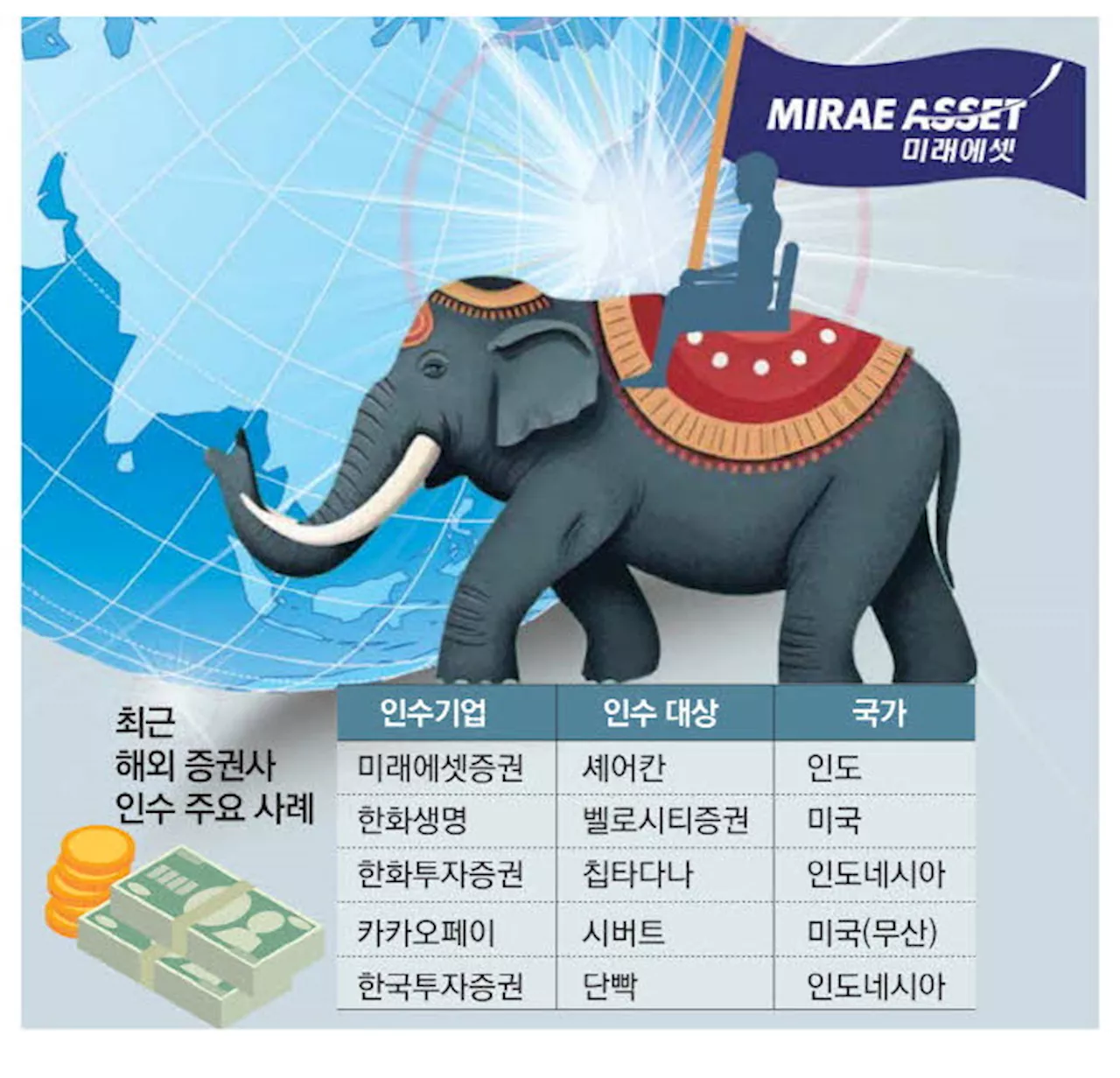 미래에셋, 인도 셰어칸證 5700억에 인수완료현지 시장점유율 8위 증권사금융당국 허가 거쳐 인수 끝내年 6% 성장 시장 공략 '가속'인도법인 고객 합치면 600만명IB·WM 등 전분야 경쟁력 확대
미래에셋, 인도 셰어칸證 5700억에 인수완료현지 시장점유율 8위 증권사금융당국 허가 거쳐 인수 끝내年 6% 성장 시장 공략 '가속'인도법인 고객 합치면 600만명IB·WM 등 전분야 경쟁력 확대
더 많은 것을 읽으십시오 »
 페덱스컵 125위→100위… PGA투어 경쟁, 더 치열해진다정책 변경안, 선수위 거쳐 정책위서 승인 2026년부터는 풀필드 대회 규모 축소 애덤 스콧 “공정한 기회, 개선된 대회 기대”
페덱스컵 125위→100위… PGA투어 경쟁, 더 치열해진다정책 변경안, 선수위 거쳐 정책위서 승인 2026년부터는 풀필드 대회 규모 축소 애덤 스콧 “공정한 기회, 개선된 대회 기대”
더 많은 것을 읽으십시오 »
 “비트코인 못샀으면 여기로 와”…가상화폐 ETF도 몸값 천정부지트럼프發 규제완화 정책 기대 서학개미도 코인 상승장 참전 가상화폐 ETF 1200억원 베팅 美 ETF 옵션상품도 승인 주목
“비트코인 못샀으면 여기로 와”…가상화폐 ETF도 몸값 천정부지트럼프發 규제완화 정책 기대 서학개미도 코인 상승장 참전 가상화폐 ETF 1200억원 베팅 美 ETF 옵션상품도 승인 주목
더 많은 것을 읽으십시오 »
 한주새 시총 57조원 증발 … 힘빠진 中빅테크習 경기부양 회의감 커진데다3분기 실적 시장 기대 못미쳐알리바바·텐센트·바이두 등주요 빅테크기업 일제히 급락항셍테크 지수도 연일 약세
한주새 시총 57조원 증발 … 힘빠진 中빅테크習 경기부양 회의감 커진데다3분기 실적 시장 기대 못미쳐알리바바·텐센트·바이두 등주요 빅테크기업 일제히 급락항셍테크 지수도 연일 약세
더 많은 것을 읽으십시오 »
